手性有机硼化合物是重要的蛋白酶抑制剂,也是重要的有机合成试剂。手性二苄基硼酸酯是一类新颖的合成砌块,可用于构建具有生物活性的偕二芳基或三芳基甲基化合物。传统合成该砌块的方法依赖于使用当量的手性底物或手性试剂;迄今为止,利用催化不对称策略合成手性二苄基硼酸酯仍是一个挑战性的课题。
成都生物研究所廖建研究小组利用课题组发展的手性亚砜烷基膦配体,首次实现了铜催化联硼酸频那醇酯对4-亚烷基苯醌的1,6-不对称加成反应,发展了一种构建手性二苄基硼酸酯的高效方法(高达97%对映选择性和97%收率)。这类新型的手性硼酸酯可方便地转化为手性醇和稳定的氟硼酸盐,后者通过Suzuki-Miyaura反应,可立体专一性(高达97%手性保持)地构建一类重要的手性三芳基甲基化合物。此外,该研究还为不对称偶联反应中的立体控制方式(手性保持或翻转)提供了一种新的思路。
研究成果以通讯形式发表在德国《应用化学》(Angew. Chem., Int. Ed. 2015, 54, doi: 10.1002/anie.201505926)上,该研究得到国家自然科学基金、中科院西部之光等课题的资助。
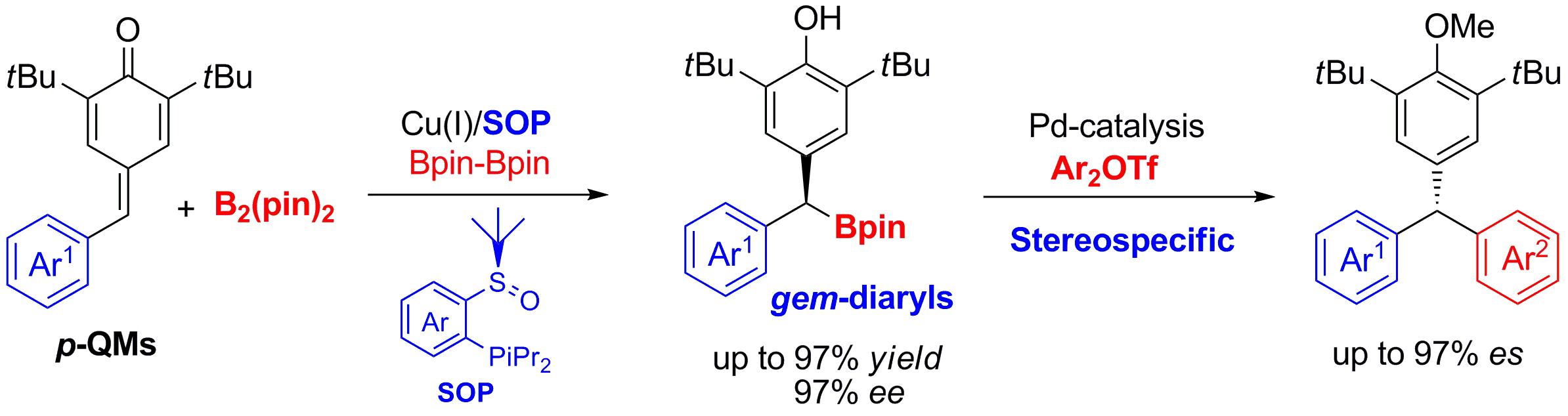
合成步骤
